Psychospołeczne i psychologiczne aspekty opieki nad pacjentami z LVAD
Życie z LVAD to nie tylko wyzwanie medyczne – to całkowita transformacja codzienności.
Urządzenie wspomagające lewą komorę serca (LVAD) ratuje życie, ale przynosi ze sobą złożone wyzwania psychiczne i społeczne. Co czwarty pacjent zmaga się z depresją, a bliscy pacjentów często odczuwają przytłaczający stres.
Dobra wiadomość? Właściwe wsparcie psychospołeczne i psychologiczne może obniżyć ryzyko zgonu nawet o 30% i dramatycznie poprawić jakość życia. Poznaj kompleksowy przewodnik oparty na najnowszych badaniach naukowych, który pokazuje, jak skutecznie zadbać o aspekty psychologiczne terapii LVAD.
Kompleksowa opieka to klucz do sukcesu.
Psychospołeczne i psychologiczne aspekty opieki nad pacjentami z LVAD
Wprowadzenie
Leczenie zaawansowanej niewydolności serca za pomocą urządzenia wspomagającego lewą komorę serca (Left Ventricular Assist Device, LVAD) znacząco wydłuża przeżycie i poprawia stan kliniczny pacjentów, jednak niesie ze sobą złożone wyzwania psychospołeczne. Badania pokazują, że około 25% pacjentów z wszczepionym LVAD doświadcza objawów depresji klinicznej, a nawet 30% odczuwa nasilony lęk.. Jednocześnie opiekunowie takich chorych – zwykle członkowie rodziny – także odczuwają olbrzymi stres: aż 69% opiekunów zgłasza wzrost poziomu stresu po implantacji LVAD. Nieleczone problemy psychiczne i brak wsparcia społecznego wpływają nie tylko na samopoczucie, ale i na wyniki leczenia. Skuteczna opieka psychospołeczna potrafi obniżyć śmiertelność pacjentów nawet o 30% oraz poprawić jakość ich życia o ponad 40%. Z tego względu kompleksowe podejście do pacjenta z LVAD – uwzględniające aspekty psychologiczne od etapu kwalifikacji aż po wieloletnią opiekę pooperacyjną – jest niezbędne, by terapia mechanicznego wsparcia serca przyniosła pełne korzyści.
Niniejsza analiza przedstawia praktyczne zalecenia oparte na najnowszych badaniach (2022–2025) dotyczące wsparcia psychospołecznego pacjentów z LVAD. Skierowana jest do szpitali, interdyscyplinarnych zespołów terapeutycznych oraz opiekunów (lekarzy, psychologów, rehabilitantów, pielęgniarek i innych) i omawia działania na etapach przedimplantacyjnym, pooperacyjnym oraz długoterminowym. Uwzględniono aktualne dane na temat depresji, lęku, stresu opiekunów, zaburzeń adaptacyjnych, postrzegania własnego ciała oraz strategii radzenia sobie z chorobą. Rekomendacje organizacyjne, systemowe i terapeutyczne opierają się na dowodach naukowych, a całość uzupełniono przykładami dobrych praktyk z Polski i zagranicy.
Warto jako wstęp przedstawić dwa wykresy.
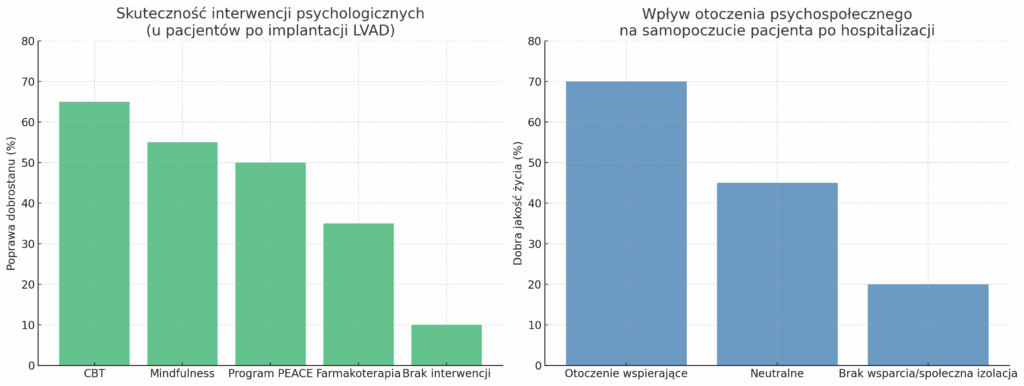
Te dwa wykresy ukazują kluczowe czynniki wpływające na jakość życia pacjentów z LVAD po wypisie ze szpitala:
📊 Skuteczność interwencji psychologicznych:
- Najwyższą skuteczność wykazuje terapia poznawczo-behawioralna (CBT) – 65% poprawy dobrostanu.
- Programy mindfulness i PEACE również dają silne efekty (50–55%).
- Sama farmakoterapia poprawia stan psychiczny u ok. 35% pacjentów, ale w połączeniu z terapią daje znacznie lepsze rezultaty.
- Brak interwencji wiąże się z minimalną poprawą (ok. 10%).
🌱 Otoczenie psychospołeczne:
- Aż 70% pacjentów z pozytywnym, wspierającym otoczeniem zgłasza dobrą jakość życia.
- W środowisku neutralnym – tylko 45%.
- W warunkach społecznej izolacji i braku wsparcia – jakość życia drastycznie spada (20%).
Główne wyzwania psychospołeczne u pacjentów z LVAD
Depresja i lęk
Pacjenci korzystający z LVAD są obciążeni wysokim ryzykiem zaburzeń nastroju i lękowych. Według badań około 20–30% chorych zgłasza istotne objawy depresyjne i lękowe – przy czym u ~19% spełniają one kryteria poważnej depresji, a u ~13% kryteria zaburzeń lękowych (np. lęku uogólnionego. Przyczyny są wieloczynnikowe. Z jednej strony istnieją mechanizmy biologiczne: przewlekła reakcja zapalna wywołana kontaktem krwi z pompą LVAD prowadzi do wzrostu cytokin prozapalnych (m.in. IL-6, TNF-α), co obniża dostępność serotoniny i dopaminy w ośrodkowym układzie nerwowym – sprzyjając rozwojowi depresji. Dodatkowo powikłania neurologiczne (np. mikro-udarowe) mogą pogarszać funkcje poznawcze i nastrój. Z drugiej strony nakładają się czynniki psychologiczne: konieczność stawienia czoła śmiertelnej chorobie serca, lęk przed zabiegiem, przed bólem, a także przed nieznaną przyszłością z urządzeniem mechanicznym w cielepsychiatriapolska.plpsychiatriapolska.pl. Pacjenci często doświadczają huśtawki emocji – od ulgi, że pojawiła się szansa na przeżycie do czasu przeszczepu, po rozczarowanie, że stan zdrowia wymaga tak radykalnej terapii pomostowejpsychiatriapolska.pl. Młodsi pacjenci (< 65 lat) mają nieraz większe trudności adaptacyjne niż starsi – czują, że tracą dotychczasową rolę społeczną i sprawność, co rodzi frustrację i obniża motywację. W efekcie depresja i lęk u chorych z LVAD są częste i wymagają systematycznego monitorowania oraz interwencji. Warto podkreślić, że wyższy poziom wewnętrznych zasobów pacjenta, takich jak samo-współczucie, może działać ochronnie – osoby bardziej samo-współczujące zgłaszają istotnie niższy lęk i depresję oraz lepsze funkcjonowanie fizycznefile-5y8tvbxuuag1xh9kdx7z6vfile-5y8tvbxuuag1xh9kdx7z6v. To wskazuje, że budowanie u pacjenta pozytywnego nastawienia do siebie i choroby stanowi ważny cel terapeutyczny.
Obciążenie i stres opiekunów.
Skuteczna terapia LVAD wymaga zaangażowania bliskich – większość ośrodków warunkuje kwalifikację pacjenta od posiadania dedykowanego opiekuna zdolnego do pomocy w opiece pooperacyjnej. Rola opiekuna bywa jednak źródłem znacznego stresu. Badania pokazują, że ponad połowa opiekunów odczuwa przeciążenie opieką, a u 69% wzrasta poziom stresu po zabiegu. W pierwszych miesiącach po implantacji u opiekunów obserwuje się skokowy wzrost napięcia (np. w jednym z badań wskaźnik obciążenia wzrósł istotnie w pierwszym miesiącu, by następnie nieco się obniżyć, ale bez powrotu do stanu wyjściowego). U części rozwijają się objawy zespołu stresu pourazowego – stwierdzono, że 26% małżonków pacjentów zakwalifikowanych do przeszczepu (BTT) spełnia kryteria PTSD. Główne źródła stresu to ogromna odpowiedzialność i konieczność nieustannej czujności, ograniczenia czasu wolnego i życia towarzyskiego, a także obciążenie fizyczne opieką nad chorym. Co ważne, kondycja opiekuna ma bezpośredni wpływ na pacjenta – brak opiekuna lub jego załamanie może skutkować przerwaniem ciągłości opieki. Pacjenci pozbawieni opiekuna mają nawet 3,1 raza wyższe ryzyko zgonu po wypisie (p=0,04). Równie niebezpieczny jest brak planu awaryjnego: jeżeli nie ma zabezpieczenia na wypadek niedyspozycji głównego opiekuna, ryzyko zgonu pacjenta wzrasta istotnie (p=0,02). Wyzwania te pokazują, że opiekunowie powinni stanowić integralny element modelu opieki – wymagają oni edukacji, wsparcia emocjonalnego i odciążenia, by móc długofalowo pełnić swoją rolę.
Obraz ciała i intymność.
Implantacja LVAD oznacza, że pacjent na stałe nosi w swoim ciele i na zewnątrz urządzenie (kabel zasilający – tzw. driveline – wyprowadzony jest przez skórę do kontrolera i baterii). Wpływa to negatywnie na postrzeganie własnego ciała – wielu chorych czuje się okaleczonych, mniej atrakcyjnych, ma trudność z akceptacją urządzenia jako części siebie. W polskim badaniu z 2025 roku wykazano, że obecność objawów lęku i depresji istotnie nasila problemy z obrazem ciała u pacjentów LVAD. Zmagają się oni z bliznami, noszeniem widocznego osprzętu, a także z obawą przed uszkodzeniem urządzenia przy codziennej aktywności. Szczególnie delikatnym obszarem jest życie intymne i seksualne. Już sam ciężki przebieg choroby serca przed implantacją często obniżał aktywność seksualną, a po zabiegu sytuacja komplikuje się przez obecność urządzenia. W badaniach 49% pacjentów zgłasza istotne zmiany w jakości życia seksualnego po LVAD – najczęściej spadek częstotliwości lub satysfakcji. Tylko 29% pacjentów z LVAD deklaruje zadowolenie ze swojego życia seksualnego, podczas gdy w grupie po przeszczepie serca odsetek ten wynosi 71% (różnica istotna, p=0,0005). Główną barierą jest lęk – obecność kabla i urządzenia budzi obawy u chorego (i partnera) przed uszkodzeniem sprzętu podczas zbliżenia. Pacjenci niepewnie czują się we własnym ciele, co hamuje spontaniczność i bliskość. Z drugiej strony, niektórzy chorzy po ustabilizowaniu stanu serca dostrzegają poprawę funkcji seksualnych dzięki lepszej wydolności krążenia oraz cenią zwiększoną bliskość z partnerem nawet bez pełnego współżycia. Wielu pacjentów chciałoby otrzymać konkretne informacje i poradę na temat bezpiecznej aktywności seksualnej – preferują np. dyskretne materiały edukacyjne na piśmie. Aspekty wizerunku ciała i seksualności są często pomijane w rutynowych wizytach, dlatego wymagana jest proaktywna postawa personelu: otwarte pytanie o te problemy, zapewnienie intymności podczas rozmowy oraz skierowanie do specjalisty (psychologa, seksuologa) jeśli pacjent/para tego potrzebuje.
Trudności adaptacyjne i radzenie sobie
Życie z LVAD wymusza wiele zmian w codziennym funkcjonowaniu, co stanowi wyzwanie adaptacyjne. Pacjent staje się zależny od urządzenia zasilanego bateriami – musi przestrzegać reżimu (ładowanie baterii, wymiana opatrunków driveline, unikanie zamoczenia urządzenia, reagowanie na alarmy). Ograniczenia te mogą prowadzić do poczucia utraty niezależności i spontaniczności. Wielu chorych obawia się awarii urządzenia lub np. przerwy w zasilaniu – żyją z ciągłym tlejącym lękiem o własne życie uzależnione od aparatury. Zdarza się unikanie aktywności społecznych z obawy, że urządzenie zwróci niepożądaną uwagę lub stanie się kłopotliwe (np. w podróży). Rodzi to poczucie osamotnienia i izolacji. Nasilona bywa także niepewność co do przyszłości – pacjenci nie wiedzą, jak długo będą żyć z LVAD, czy doczekają transplantacji, co wywołuje przewlekły stres porównywalny z życiem „w zawieszeniu”. Radzenie sobie z tym stresem zależy od indywidualnych zasobów i strategii. Jako strategie adaptacyjne pacjenci często stosują podejście zadaniowe: uczą się skrupulatnie obsługiwać LVAD, koncentrują na harmonogramie pomiarów i procedur – to radzenie sobie skoncentrowane na problemie, które zwiększa poczucie kontroli nad sytuacjąfile-loesf2rt6rekhsjfhyskxu. Równolegle istotne są strategie emocjonalne: wielu chorych stara się zachować pozory normalności – poprzez zdystansowanie się od myśli o chorobie, drobne aktywności odwracające uwagę (hobby, spotkania online), czy pozytywne przewartościowanie („cieszę się każdą chwilą, którą dał mi LVAD”)file-loesf2rt6rekhsjfhyskxu. Badania jakościowe pokazują, że pacjenci stosują auto-perswazję i dystrakcję, by zintegrować LVAD ze swoim życiem i tożsamościąfile-loesf2rt6rekhsjfhyskxu. Niemniej, adaptacja nie u wszystkich przebiega pomyślnie – część chorych pozostaje w stanie chronicznego napięcia i niepokoju, co pogarsza ich jakość życia, a nawet może wpływać na wyniki leczenia (np. nieadekwatna obsługa urządzenia, zaniedbywanie zaleceń). Przykładowo, pacjenci cechujący się wysokim ryzykiem psychospołecznym (ograniczone wsparcie, zaburzenia poznawcze, nałogi, ciężka choroba psychiczna lub skłonność do nieprzestrzegania zaleceń) stanowią ok. 20% populacji LVAD – badanie INTERMACS wykazało, że obecność takich czynników ryzyka wiąże się z istotnie częstszymi powikłaniami: infekcjami, krwawieniami, zakrzepicą pomp i rehospitalizacjamipubmed.ncbi.nlm.nih.govpubmed.ncbi.nlm.nih.gov. Co ważne, samo przeżycie nie różniło się tu istotnie, co sugeruje, że nawet pacjenci z problemami psychospołecznymi mogą żyć długo z LVAD, o ile otrzymają odpowiednie wsparciepubmed.ncbi.nlm.nih.gov. Podsumowując, wyzwania adaptacyjne pacjentów z LVAD są wielowymiarowe – obejmują sferę emocji, tożsamości, relacji społecznych i praktycznych umiejętności. Zidentyfikowanie tych trudności u danego pacjenta pozwala zaplanować interwencje (np. trening radzenia sobie, pomoc psychologiczną, grupy wsparcia), które ułatwią zaakceptowanie nowej rzeczywistości.
Opieka psychospołeczna przed implantacją LVAD
Efektywne wsparcie pacjenta z LVAD rozpoczyna się jeszcze przed zabiegiem, na etapie kwalifikacji. Międzynarodowe wytyczne (np. ISHLT 2023) zalecają, aby każdy kandydat do LVAD przeszedł wszechstronną ocenę psychospołeczną. Celem takiej oceny jest identyfikacja czynników mogących zagrozić pomyślnemu przebiegowi terapii bądź adaptacji pacjenta, w tym: brak wsparcia społecznego (samotność pacjenta), niezdolność intelektualna lub zaburzenia poznawcze utrudniające współpracę, aktywne uzależnienia (alkohol, narkotyki), nieleczone poważne choroby psychiczne (np. depresja ciężka, psychozy) oraz skłonność do nieprzestrzegania zaleceń leczeniapubmed.ncbi.nlm.nih.govpubmed.ncbi.nlm.nih.gov. W praktyce wiele ośrodków korzysta z ustrukturyzowanych narzędzi oceny – np. Stanford Integrated Psychosocial Assessment for Transplantation (SIPAT) lub zmodyfikowanej skali PACT – które pozwalają przypisać pacjentowi profil ryzyka psychospołecznego i przewidzieć m.in. prawdopodobieństwo nieplanowanych rehospitalizacji. Standardowo wykonuje się skale przesiewowe: PHQ-9 dla depresji, GAD-7 dla lęku (przy czym już wyniki ≥5 pkt wskazują na potrzebę dalszej oceny). Ocena powinna też obejmować akceptację przyszłego urządzenia (pomaga tu kwestionariusz FPAS – Florida Patient Acceptance Survey) oraz nasilenie poczucia osamotnienia (np. skrócona skala samotności UCLA). Jeśli pacjent jest w związku, warto porozmawiać z partnerem/rodziną o spodziewanych zmianach, w tym o sferze intymnej – można posłużyć się np. kwestionariuszem SALVADOR, który ocenia obawy związane z seksualnością przy LVAD.
Równie istotnym elementem kwalifikacji jest ocena gotowości i możliwości opiekuna. Należy upewnić się, że pacjent ma wyznaczoną osobę (lub zespół osób) gotowych pełnić rolę opiekuna 24/7, i że osoby te rozumieją, na czym polega opieka przy LVAD. Już na tym etapie warto zaangażować opiekuna w proces edukacji – omawiać wspólnie z pacjentem i rodziną plan leczenia, oczekiwania i potencjalne obciążenia. Jeśli kandydat nie ma żadnego wsparcia społecznego, zespół powinien rozważyć alternatywy (np. opiekę instytucjonalną, pomoc społeczną) lub niestety – odroczenie zabiegu. Badania jasno pokazują, że brak opiekuna stanowi przeciwwskazanie względne do LVAD, gdyż zagraża bezpieczeństwu chorego.
Interwencje przedoperacyjne
Poza selekcją pacjentów pod kątem ryzyka, niezwykle ważne jest przygotowanie psychiczne chorego do życia z LVAD. W polskich ośrodkach praktykuje się udział psychologa klinicznego na etapie kwalifikacji – jego zadaniem jest edukacja i wsparcie emocjonalne pacjenta przed operacjąpsychiatriapolska.pl. Jak opisują eksperci, przygotowanie to obejmuje: wyjaśnienie pacjentowi, jakie zmiany stylu życia niesie LVAD (np. reżim higieniczny, ograniczenia w kąpieli, stała obecność baterii), pomoc w przepracowaniu lęków (przed operacją, bólem, śmiercią) oraz korygowanie ewentualnych błędnych przekonańpsychiatriapolska.plpsychiatriapolska.pl. Pacjent uczy się technik radzenia sobie ze stresem – np. ćwiczy metody relaksacji przed zabiegiem, techniki odwracania uwagi od negatywnych myśli. Jeśli występują jawne zaburzenia psychiczne (np. epizod depresyjny reaktywny na pogorszenie stanu serca), rozpoczyna się ich leczenie jeszcze przed implantacją – farmakologiczne i/lub psychoterapeutycznepsychiatriapolska.pl. Często spotykane są zaburzenia adaptacyjne z lękiem – wówczas krótkoterminowo można rozważyć wsparcie farmakologiczne (np. małe dawki benzodiazepin przed operacją na silny lęk), choć ostrożnie by nie nasilić ryzyka delirium pooperacyjnego. Jeżeli wdraża się antydepresant, należy pamiętać o interakcjach z leczeniem okołooperacyjnym. Wszyscy pacjenci z LVAD wymagają przewlekłej antykoagulacji warfaryną (INR docelowo 2,0–3,0) oraz aspiryną. Wybór leku przeciwdepresyjnego musi uwzględniać wpływ na krzepnięcie – SSRI i SNRI mogą zwiększać ryzyko krwawień, więc konieczne jest monitorowanie INR przy każdej zmianie dawki. Zalecane są preparaty o mniejszym potencjale interakcji z układem CYP450, np. sertralina czy escitalopram, które uważane są za bezpieczniejsze w tej grupie. Z kolei bezwzględnie przeciwwskazane są nowoczesne doustne antykoagulanty (NOAC) u pacjentów z LVAD, więc jeśli pacjent stosował je wcześniej, trzeba przejść na warfarynę. Oczywiście każdy przypadek wymaga konsultacji psychiatrycznej i planu dostosowanego do pacjenta.
Kluczowym elementem przygotowania jest również szkolenie pacjenta i opiekuna. Najlepsze ośrodki prowadzą przedoperacyjne warsztaty, podczas których omawia się budowę i działanie LVAD, zasady pielęgnacji, postępowanie w sytuacjach awaryjnych (alarmy urządzenia, zasilanie zapasowe itp.)isbzdrowie.pl. Taka edukacja techniczna, połączona z rozmową o obawach pacjenta, znacząco zmniejsza lęk przed nieznanym i buduje współpracę. Pacjent powinien poznać innych chorych po LVAD – czy to osobiście, czy przez materiały (np. historie pacjentów „ekspertów przez doświadczenie”). Polska strona internetowa jednego ze szpitali implantujących LVAD przytacza słowa pacjenta: „Sukces jest w głowie” – podkreślając, że pozytywne nastawienie i wiedza pomogły mu przetrwać trudny czas z pompąszpitaljp2.krakow.pl. To pokazuje, jak ważne jest wzmacnianie nadziei i nastawienia pacjenta na współpracę – wiary, że poradzi sobie z urządzeniem i odzyska kontrolę nad życiem.
Opieka psychospołeczna po implantacji i w opiece długoterminowej
Okres szpitalny po operacji
Pierwsze dni i tygodnie po implantacji LVAD są dla pacjenta niezwykle trudne zarówno fizycznie, jak i psychicznie. W tym czasie priorytetem zespołu jest ustabilizowanie stanu somatycznego chorego, ale równolegle należy zadbać o jego kondycję psychiczną. Wiele osób doświadcza przeładowania bodźcami – pobyt na OIOM-ie, otoczenie aparatury, dolegliwości bólowe i uboczne skutki leków (np. zaburzenia snu, splątanie) mogą wywoływać epizody ostrego delirium lub silnego niepokoju. Zaleca się regularne wizyty psychologa lub psychoterapeuty przy łóżku pacjenta, począwszy od momentu, gdy tylko stan świadomości na to pozwala. Krótkie rozmowy ukierunkowane na uspokojenie pacjenta, wyjaśnienie mu aktualnej sytuacji oraz zapewnienie, że najtrudniejszy etap ma za sobą – mają dużą wartość terapeutyczną. Jeżeli pacjent przejawia objawy pourazowe (np. natrętne wspomnienia zatrzymania krążenia czy intensywnej terapii), warto rozważyć zastosowanie technik odwrażliwiania traumy, takich jak EMDR (Eye Movement Desensitization and Reprocessing). Metoda ta – uznana przez WHO od 2013 r. jako terapia oparta na dowodach – okazała się skuteczna w przetwarzaniu traumatycznych przeżyć związanych z hospitalizacją i samą implantacją urządzenia. Już kilka sesji EMDR przeprowadzonych na wczesnym etapie rekonwalescencji może zapobiec rozwojowi pełnoobjawowego PTSD u pacjenta. Podobnie, techniki mindfulness (uważności) warto wprowadzać, gdy tylko chory jest w stanie uczestniczyć – nawet krótkie ćwiczenia oddechowe i trening skupienia uwagi pomagają redukować stres i ból, co potwierdzono badaniami nad interwencjami MBSR/MBCT u pacjentów kardiologicznych. Wczesna rehabilitacja również przynosi korzyści psychologiczne – stopniowe pionizowanie i chodzenie z fizjoterapeutą budują w pacjencie poczucie sprawczości i poprawiają nastrój dzięki uwalnianiu endorfin. W jednym z badań 4-tygodniowy program usprawniania szpitalnego przyniósł u chorych z LVAD znaczną poprawę jakości życia już w momencie wypisu, porównywalną z poprawą obserwowaną u pacjentów po transplantacji serca. Co więcej, po kolejnych 3 miesiącach u pacjentów LVAD odnotowano dalszą poprawę wydolności (6-minutowy test chodu) oraz subiektywnego samopoczucia – w tym złagodzenie odczuwanych objawów niewydolności serca i bólu. Wyniki te wskazują, że kompleksowa rehabilitacja kardiologiczna, będąca standardem po przeszczepie, jest równie potrzebna i skuteczna u chorych z LVAD. Dlatego dobrą praktyką jest kierowanie pacjentów po stabilizacji stanu do specjalistycznego ośrodka rehabilitacji kardiologicznej, gdzie kontynuowana jest praca nad wydolnością fizyczną, ale też edukacja i wsparcie psychologiczne.
Przygotowanie do wypisu.
Zanim pacjent opuści szpital z urządzeniem, zespół powinien upewnić się, że zarówno on sam, jak i opiekun, czują się pewnie w obsłudze LVAD i radzeniu sobie na co dzień. Stosuje się check-listy kompetencji – pacjent i opiekun uczą się m.in. zmiany baterii, reagowania na alarm dźwiękowy, czyszczenia miejsca wyprowadzenia driveline, rozpoznawania objawów infekcji itp. Dobrym standardem jest przekazanie pacjentowi materiałów edukacyjnych (instrukcje, poradniki, kontakty alarmowe) w przystępnej formie. Koordynator LVAD (zwykle specjalnie przeszkolona pielęgniarka) organizuje sesję szkoleniową, często z symulacją sytuacji awaryjnych. Przed wypisem warto zorganizować spotkanie pacjenta (lub kontakt telefoniczny) z innym pacjentem żyjącym z LVAD – taki mentoring rówieśniczy dodaje otuchy i pozwala wymienić praktyczne wskazówki (np. jak podróżować z urządzeniem, jak zorganizować sobie dzień). Niezbędne jest też ustalenie planu opieki ambulatoryjnej: najbliższa wizyta kontrolna (zwykle 1–2 tygodnie po wypisie) oraz planowany stały monitoring stanu psychicznego. Pacjent powinien otrzymać informację, że w razie pojawienia się silnego przygnębienia, lęku czy myśli rezygnacyjnych – ma zgłosić to lekarzowi lub psychologowi, a nie ukrywać. Należy otwarcie omówić temat myśli samobójczych – choć skrajnie rzadko, zdarzały się próby samobójcze u pacjentów z LVAD, stąd każdorazowo trzeba ocenić ryzyko autoagresji i zabezpieczyć broń palną/leki w otoczeniu chorego, jeśli byłoby to zasadne. W praktyce jednak zdecydowana większość pacjentów, opuszczając szpital, jest pełna nadziei i wdzięczności za „drugie życie”. Rolą zespołu jest tę nadzieję podtrzymać, ale i przygotować na wyzwania – stąd zalecenie, by jeszcze przed wypisem zorganizować wspólne spotkanie z pacjentem i jego opiekunem celem podsumowania dotychczasowych postępów, rozwiania ostatnich wątpliwości i podkreślenia dostępnych form wsparcia.
Ambulatoryjna opieka długoterminowa.
Pacjent z LVAD wymaga ścisłego nadzoru po opuszczeniu szpitala – zarówno medycznego, jak i psychospołecznego. Najbardziej efektywnym podejściem, rekomendowanym w wielu krajach, jest model opieki skoordynowanej („shared care”). Polega on na ścisłej współpracy ośrodka implantującego LVAD z lokalnymi jednostkami (np. poradniami kardiologicznymi bliżej miejsca zamieszkania pacjenta). Optymalny harmonogram wygląda następująco: pacjent bezpośrednio po wypisie jest kontrolowany co 1–2 tygodnie w ośrodku wszczepiającym (lub pozostaje tam na rehabilitacji stacjonarnej), następnie – jeśli stan jest stabilny – część wizyt kontrolnych przejmuje ośrodek lokalny według ustalonych protokołów, przy stałej komunikacji z centrum specjalistycznym. Na wizytach kontrolnych ocenia się nie tylko parametry medyczne (pomiar ciśnienia, badania krwi, kontrola działania urządzenia, ew. ECHO serca), ale za każdym razem powinien odbyć się przesiew stanu psychicznego. Minimum to wypełnienie przez pacjenta krótkich skal depresji i lęku (PHQ-9, GAD-7) oraz rozmowa pielęgniarki/lekarza o samopoczuciu. Jeżeli wyniki wskazują na pogorszenie nastroju lub inne problemy, należy skierować chorego do specjalisty zdrowia psychicznego (psychologa lub psychiatry). W ramach opieki długoterminowej zaleca się również okresowe badanie akceptacji urządzenia – np. powtórne użycie kwestionariusza FPAS po 6 czy 12 miesiącach, by zobaczyć, czy pacjent lepiej radzi sobie z LVAD, czy też narastają u niego negatywne odczucia (frustracja, poczucie stygmatyzacji urządzeniem). Spadek akceptacji mógłby zapowiadać np. gorszą współpracę pacjenta czy ryzyko depresji – warto wtedy zintensyfikować wsparcie. Równolegle monitorujemy opiekuna: podczas wizyt pytamy, jak radzi sobie w swojej roli, czy nie potrzebuje pomocy. W niektórych ośrodkach opiekunowie również wypełniają prosty kwestionariusz obciążenia opieką – co pozwala wyłapać osoby szczególnie przeciążone i zaproponować im interwencje (np. poradnictwo psychologiczne, kontakt z grupą wsparcia dla opiekunów).
Interwencje terapeutyczne po implantacji.
W zależności od potrzeb danego pacjenta, w okresie pooperacyjnym można wdrożyć różne formy pomocy psychologicznej:
- Psychoterapia indywidualna (najczęściej poznawczo-behawioralna) jest złotym standardem leczenia depresji i lęku u pacjentów kardiologicznych, w tym z LVAD. Metaanalizy potwierdzają, że CBT (terapia poznawczo-behawioralna) osiąga średni i duży efekt w redukcji objawów (d Cohena = 0,6–0,8), a połączenie psychoterapii z farmakoterapią jest skuteczniejsze niż samo podawanie leków. W praktyce program terapii CBT dla pacjentów z LVAD powinien być dostosowany do ich specyficznych problemów. Terapeuta pracuje nad akceptacją urządzenia – pomaga zmienić myślenie pacjenta o LVAD z wroga odbierającego wolność na sprzymierzeńca podtrzymującego życie. Wspólnie identyfikują zniekształcenia poznawcze (np. katastroficzne myśli „jak tylko zostanę sam, na pewno urządzenie się zepsuje i umrę”) i dokonują ich restrukturyzacji – to znaczy poszukują bardziej zrównoważonych przekonań (np. „urządzenie jest niezawodne, mam zapasowe baterie, a w razie czego opiekun wezwie pomoc”). Ważnym modułem jest trening umiejętności społecznych i rozwiązywania problemów – pacjent ćwiczy np. jak komunikować się z personelem medycznym, gdy czegoś potrzebuje, albo jak wytłumaczyć obcej osobie w przestrzeni publicznej czym jest jego urządzenie, by czuć się swobodniej wśród ludzi. Bardzo istotna jest praca nad samotnością – wielu pacjentów z LVAD czuje się wyobcowanych, stąd terapeuta zachęca do odbudowy relacji (choćby w nowej formie, np. zdalnie) i uczy technik radzenia sobie z uczuciem osamotnienia. Wreszcie, stałym elementem terapii powinna być profilaktyka nawrotów – ustalenie planu działania na wypadek pogorszenia nastroju w przyszłości, sygnałów ostrzegawczych i strategii szukania pomocy. W niektórych ośrodkach wdraża się ustrukturyzowane programy CBT dla pacjentów z LVAD trwające np. 12 sesji (1 raz w tygodniu przez ~3 miesiące), obejmujące wspomniane moduły od edukacji, przez zmianę myślenia i zachowań, po zapobieganie nawrotom.
- Interwencje oparte na mindfulness i terapii traumy – wspomniane wcześniej techniki uważności (mindfulness) stosowane są także ambulatoryjnie w formie programów MBSR (Mindfulness-Based Stress Reduction) czy MBCT (Mindfulness-Based Cognitive Therapy). Pacjenci uczą się medytacji, skupienia na „tu i teraz”, co pomaga im obniżyć przewlekły stres związany z życiem z LVAD i łagodzić reakcje lękowe. Wykazano, że praktyka mindfulness może modulować nadreaktywność układu nerwowego (np. obniżać poziom prozapalnej aktywacji mikrogleju) i tym samym korzystnie wpływać na nastrój. W przypadku pacjentów, którzy przeszli wyjątkowo traumatyczne doświadczenia (np. długa reanimacja, wielotygodniowy pobyt na OIOM), warto kontynuować terapię traumy – EMDR lub innymi metodami (np. przedłużona ekspozycja) – aż do przepracowania tych przeżyć.
- Interwencje z obszaru psychologii pozytywnej i budowania rezyliencji (odporności psychicznej). Coraz więcej badań wskazuje, że oprócz redukcji negatywnych objawów warto równolegle wzmacniać pozytywne zasoby pacjenta. Programy interwencyjne oparte na psychologii pozytywnej (tzw. Positive Psychology Interventions, PPI) skupiają się na rozwijaniu u pacjenta uczuć wdzięczności, nadziei, poczucia sensu i korzystaniu z posiadanych zalet charakteru. Przykładem jest program PEACE opisany w 2022 r., w którym pacjenci LVAD uczestniczyli w 8 sesjach (prowadzonych telefonicznie) poświęconych praktykowaniu wdzięczności, życzliwości i identyfikowaniu swoich mocnych stron. Wyniki takiej interwencji były obiecujące – odnotowano u uczestników spadek objawów depresji i stresu oraz wzrost odczuwanej satysfakcji z życia i emocji pozytywnych. Choć badanie było pilotażowe (niewielka grupa), wpisuje się w szerszą tendencję: łączenie klasycznych oddziaływań klinicznych z podejściem ukierunkowanym na dobrostan. Budowanie odporności psychicznej (rezyliencji) można też realizować poprzez grupowe warsztaty dla pacjentów – uczące znajdowania radości w małych rzeczach, planowania przyszłości pomimo niepewności czy podtrzymywania aktywności dających poczucie sensu. Takie eudajmonistyczne podejście pomaga pacjentom nie tylko przeżyć, ale i dobrze żyć z LVAD, przekierowując uwagę z choroby na cele i wartości osobiste.
- Terapia par i poradnictwo rodzinne. Z uwagi na wpływ LVAD na całą rodzinę, często wskazane jest objęcie wsparciem psychologicznym również bliskich pacjenta – przede wszystkim partnera życiowego. Tematy do przepracowania to m.in.: redystrybucja ról w rodzinie (np. pacjent z powodu ograniczeń mniej pracuje zawodowo, za to partner przejmuje więcej obowiązków – może to rodzić napięcia i frustracje po obu stronach), komunikacja o chorobie (otwarte wyrażanie uczuć, żeby unikać nieporozumień), a także życie seksualne. W specjalistycznych centrach (np. kliniki niemieckie czy amerykańskie) prowadzi się edukacyjne sesje dla par dotyczące bezpiecznej aktywności seksualnej z LVAD oraz radzenia sobie z obniżonym libido czy zmianą sposobu okazywania bliskości. Zapewnienie komfortu psychicznego w tej sferze przekłada się na ogólną jakość życia obojga partnerów, stąd nie powinno być tabu. Ponadto opiekunowie mogą skorzystać z grup wsparcia dla rodzin pacjentów z LVAD – wymiana doświadczeń z innymi opiekunami często przynosi ulgę (uczucie „nie jesteśmy sami w tej sytuacji”).
- Kontrola i profilaktyka uzależnień. U pacjentów z historią nadużywania alkoholu czy innych substancji należy utrzymać wzmożoną czujność w okresie pooperacyjnym. Stres związany z chorobą i nowymi obowiązkami może prowokować nawroty nałogu, które w kontekście LVAD są szczególnie niebezpieczne (np. upojenie alkoholowe może skutkować zaniedbaniem opieki nad urządzeniem lub interakcją z lekami). Standardem jest regularny skrining nawyków – np. za pomocą krótkiego testu AUDIT-C przy każdej wizycie (3 pytania oceniające picie alkoholu). Co ciekawe, wykazano, że AUDIT-C ma porównywalną czułość do pełnego 10-pytaniowego AUDIT w wykrywaniu problemowego picia – sugerowane punkty odcięcia to ≥4 dla mężczyzn i ≥3 dla kobiet. Jeśli pacjent wróciłby do nałogu, wymaga natychmiastowej interwencji – od intensywnej psychoedukacji po skierowanie na terapię uzależnień i pomoc w jej znalezieniu, terapię zaburzeń mogących współistnieć z uzależnieniem, aż po czynniki psychospołeczne wymienione w późnych powikłaniach pooperacyjnych w instrukcji HM3, które mogą utrudniać epizody spożywania substancji. Warto zauważyć, że sama przeszłość uzależnienia nie musi przekreślać sukcesu LVAD – analizy wskazują, że choć nie zwiększa ona istotnie śmiertelności, to jednak podnosi ryzyko powikłań mechanicznych (zakrzepy w pompach, infekcje) i wydłuża pobyty w szpitalu.
Dlatego utrzymanie abstynencji i zdrowych nawyków jest jednym z celów długoterminowej opieki psychospołecznej.
Wsparcie telemedyczne i społecznościowe. W dobie technologii cyfrowych coraz większą rolę odgrywa teleopieka i platformy online. Pacjentom z LVAD można proponować konsultacje z psychologiem poprzez wideorozmowy, co jest szczególnie wartościowe, gdy mieszkają daleko od ośrodka lub mają ograniczoną mobilność. Ponadto istnieją globalne internetowe grupy wsparcia pacjentów z LVAD oraz profile na portalach społecznościowych, gdzie chorzy i ich rodziny dzielą się radami. Trzeba jednak pamiętać, że interwencje cyfrowe nie zastąpią bezpośredniego kontaktu – badania wskazują, że same aplikacje czy czaty mają ograniczoną skuteczność jako jedyne źródło wsparcia. Najlepsze efekty daje połączenie – np. pacjent korzysta z aplikacji do monitorowania nastroju, ale ma regularny kontakt z terapeutą, który analizuje te dane (tzw. blended care). Ważne jest też zapewnienie pacjentom prostych kanałów kontaktu z kliniką – np. czynnego całą dobę numeru telefonu do koordynatora LVAD, pod który można zgłosić zarówno problem techniczny, jak i skonsultować nagłe pogorszenie nastroju czy inne niepokojące objawy psychiczne.
Zalecenia organizacyjne i systemowe
Wprowadzenie kompleksowej opieki psychospołecznej nad pacjentami z LVAD wymaga wsparcia na poziomie organizacji służby zdrowia oraz zespołów terapeutycznych. Poniżej zebrano kluczowe rekomendacje:
- Multidyscyplinarny zespół LVAD: Każdy ośrodek implantujący i prowadzący chorych z LVAD powinien dysponować zespołem wielodyscyplinarnym, w którego skład wchodzą nie tylko kardiochirurdzy i kardiolodzy, ale także specjaliści innych dziedzin: perfuzjoniści (obsługa techniczna pomp), anestezjolodzy i intensywiści, pielęgniarki, rehabilitanci, dietetyk, specjalista chorób zakaźnych, psycholog kliniczny i/lub psychiatra, pracownik socjalny oraz koordynatorzy opieki LVAD. Najnowsze wytyczne ISHLT (2023) jednoznacznie wskazują konieczność zaangażowania eksperta zdrowia psychicznego w podstawowy zespół opieki nad pacjentem z LVAD. Ponadto zaleca się regularne spotkania interdyscyplinarne tego zespołu – omawianie przypadków, wspólne szkolenia – co sprzyja wymianie wiedzy i podnoszeniu jakości opieki.
- Stałe szkolenia i podnoszenie kompetencji: Personel medyczny powinien przechodzić cykliczne szkolenia z zakresu opieki nad pacjentami LVAD, obejmujące również komponent psychospołeczny. ISHLT rekomenduje trójfazowe programy szkoleniowe: Faza I (podstawowa) – kilkumiesięczne wprowadzenie, gdzie wszyscy członkowie zespołu poznają podstawy terapii LVAD, komunikacji z pacjentem i protokoły bezpieczeństwa; Faza II (specjalizacyjna) – dalsze 6 miesięcy rozwijania zaawansowanych umiejętności (rozwiązywanie złożonych problemów klinicznych, udział w badaniach naukowych); Faza III (ciągłe doskonalenie) – coroczna ocena kompetencji, obowiązkowa edukacja ciągła, warsztaty z omawianiem przypadków trudnych. Taki system gwarantuje, że zespół stale podnosi swoje kwalifikacje, a co za tym idzie – jakość opieki.
- Standaryzacja protokołów opieki psychospołecznej: W każdym ośrodku należy opracować pisemne protokoły postępowania uwzględniające aspekt psychospołeczny. Powinny one obejmować: harmonogram skriningu (jakie narzędzia i kiedy stosować u pacjentów i opiekunów), ścieżkę postępowania w razie wykrycia ryzyka samobójczego lub poważnego kryzysu psychicznego (np. pilna konsultacja psychiatryczna, możliwość hospitalizacji na oddziale psychiatrycznym), zasady kierowania na psychoterapię lub rehabilitację psychiatryczną. Standardowy protokół może zakładać np.: ocenę nastroju i lęku przy każdej wizycie ambulatoryjnej, rutynową psychoedukację (przez lekarza lub pielęgniarkę) dotyczącą radzenia sobie ze stresem, i w razie potrzeby – skierowanie do specjalisty zdrowia psychicznego wraz z pomocą w znalezieniu takiego oraz ustalenie częstszego follow-upu. Dla pacjentów z grup ryzyka (np. wcześniejsze choroby psychiczne) warto wdrożyć protokoły zaawansowane – obejmujące jeszcze przed implantacją pełną ocenę psychologiczną, włączenie zaplanowanej psychoterapii zaraz po zabiegu, objęcie wsparciem psychologicznym także opiekunów oraz organizację programów wsparcia rówieśniczego (np. spotkania z innymi pacjentami). Protokół zaawansowany powinien zakładać długoterminowy nadzór co najmniej 2 lata po implantacji, bo tyle zwykle trwa pełna adaptacja.
- Model opieki dzielonej (shared care): Jak wspomniano, współpraca między centrum implantującym a lekarzami lokalnymi jest kluczowa. Pacjent po powrocie do domu często ma bliżej do swojego kardiologa prowadzącego – warto, aby ten kardiolog został włączony w plan opieki i przeszkolony w podstawach postępowania z LVAD. Model shared care zakłada podpisanie formalnych porozumień między ośrodkiem referencyjnym a szpitalami rejonowymi: określa się podział odpowiedzialności (kto i gdzie wykonuje które badania i kontrole), zasady komunikacji (np. regularne telekonferencje w celu omówienia stanu pacjenta, szybka ścieżka przekazywania pacjenta z powrotem do centrum w razie komplikacji). Korzyści z takiego modelu to m.in.: zmniejszenie obciążenia ośrodków specjalistycznych nadmiarem wizyt kontrolnych, zapewnienie pacjentowi opieki wysokiej jakości bliżej domu, redukcja kosztów i uciążliwości transportu chorego oraz lepsza ciągłość opieki (pacjent czuje, że jest zaopiekowany w każdym miejscu). Warunkiem sukcesu jest jednak dobra komunikacja i standaryzacja – lokalny zespół musi dokładnie wiedzieć, jakie procedury wykonać, a w razie wątpliwości mieć łatwy kontakt z centrum. W krajach takich jak Niemcy czy Holandia wypracowano sieć ośrodków satelitarnych współpracujących z klinikami LVAD – Polska może czerpać z tych doświadczeń, adaptując je do realiów (np. uwzględniając strukturę oddziałów kardiologicznych i rolę poradni przyszpitalnych).
- Zapewnienie finansowania i wsparcia systemowego: Kompleksowa opieka psychospołeczna wymaga nakładów – etatów dla psychologów, szkolenia personelu, programów rehabilitacji, grup wsparcia itp. NFZ powinien uwzględniać te elementy w wycenie procedur związanych z LVAD. Wdrożenie nowego modelu opieki może wymagać systemowych zmian, ale jest inwestycją, która się opłaca. Analizy ekonomiczne pokazują, że choć sam zabieg wszczepienia LVAD jest bardzo kosztowny (200–300 tys. euro), to dodatkowe koszty programów psychospołecznych są znikome w porównaniu z potencjalnymi oszczędnościami. Przykładowo, program profilaktyki uzależnień i wsparcia psychologicznego może kosztować ok. 5–10 tys. euro na pacjenta, ale jeśli dzięki niemu unikniemy choć jednej poważnej komplikacji (zakrzepica pompy, infekcja) wymagającej rehospitalizacji, oszczędności przewyższają ten wydatek. Pacjenci z nieleczonymi problemami psychospołecznymi mają prawie 80% wyższy wskaźnik ponownych hospitalizacji i średnio o 8 dni dłuższe pobyty w przypadku komplikacji. Do tego dochodzą koszty pośrednie: utracona produktywność (szacowana na 40–60 tys. euro rocznie na pacjenta w zaawansowanej niewydolności), obciążenie członków rodziny (absencje w pracy z powodu opieki, koszty opieki zastępczej). Inwestycja w opiekę psychologiczną jest więc nie tylko etycznie słuszna, ale i ekonomicznie zasadna – poprawiając wyniki leczenia, obniża łączne koszty terapii. Rekomenduje się, aby decydenci ochrony zdrowia w Polsce czerpali z doświadczeń krajów zachodnich (Niemiec, Holandii, Francji), gdzie systemy opieki nad pacjentami z LVAD są bardziej dojrzałe i uwzględniają finansowanie długofalowego wsparcia psychospołecznego.
- Monitorowanie i ciągłe usprawnianie jakości opieki: Każdy program opieki nad pacjentami z LVAD powinien podlegać regularnej ocenie skuteczności. Zaleca się śledzenie wskaźników takich jak: częstość rehospitalizacji z przyczyn psychosomatycznych, wyniki jakości życia pacjentów (np. w kwestionariuszu KCCQ), poziom depresji/lęku w populacji pod opieką, satysfakcja pacjentów i opiekunów ze wsparcia psychospołecznego. Dzięki temu można identyfikować obszary wymagające poprawy (np. jeśli mimo interwencji pacjenci nadal czują się samotni, może warto zorganizować formalne grupy spotkaniowe). Dobre praktyki to np. ankiety anonimowe wypełniane przez pacjentów i rodziny na temat ich doświadczeń z opieką – pozwalają one wprowadzać zmiany bardziej zorientowane na potrzeby chorych.
Przykłady dobrych praktyk
Polska: W Polsce terapia LVAD wciąż się rozwija, ale mamy już kilka ośrodków z dużym doświadczeniem (Zabrze, Kraków, Warszawa, Wrocław). Przykładowo, w Krakowskim Szpitalu Specjalistycznym im. Jana Pawła II – jednym z nielicznych w Polsce implantujących LVAD – od lat działa zespół psychologów opiekujących się pacjentami oczekującymi na transplantację i wspomaganie mechanicznemp.pl. Stworzono tam program wsparcia, w ramach którego pacjenci jeszcze przed operacją uczestniczą w konsultacjach psychologicznych przygotowujących do zmiany stylu życia i uczących radzić sobie ze stresem. Wspomniany wcześniej artykuł w Psychiatrii Polskiej to wynik współpracy specjalistów z Krakowa i Zabrza – jest dowodem, że polskie ośrodki dostrzegają wagę aspektów psychicznych i dzielą się wiedzą, by ujednolicić standardy opiekipsychiatriapolska.pl. Coraz częściej pacjenci z LVAD mają możliwość kontynuowania rehabilitacji psychologicznej w sanatoriach kardiologicznych (np. w ramach prewencji rentowej ZUS). Pewnym wyzwaniem pozostaje finansowanie – brakuje dedykowanych świadczeń NFZ dla wsparcia psychologicznego pacjentów kardiologicznych, ale można korzystać ze świadczeń ogólnych (psycholog w poradni kardiologicznej lub psychiatrycznej). Ważne, aby kierownictwa szpitali tworzyły etaty lub angażowały psychologów w zespołach LVAD – bez tego trudno o ciągłość opieki. Pozytywnym sygnałem jest fakt, że w dokumentach urzędowych (np. wytyczne konsultantów) coraz częściej pojawiają się zapisy o potrzebie oceny psychologicznej przed kwalifikacją do LVAD, co formalizuje ten element opieki.
Zagranica: W krajach o dłuższej historii programów LVAD wypracowano wiele sprawdzonych rozwiązań. Niemcy – posiadają rozbudowaną sieć ośrodków LVAD i programów rehabilitacji: pacjent po wypisie zazwyczaj trafia na 3-tygodniową rehabilitację stacjonarną opłacaną z ubezpieczenia, gdzie pod opieką psychologów i terapeutów zajęciowych uczy się funkcjonować z urządzeniem. W klinice w Oldenburgu prowadzono cytowane wcześniej badania jakościowe z udziałem pacjentów żyjących >10 lat z LVAD – wnioski autorów wskazują na konieczność opracowania specyficznych programów wsparcia długoterminowego, zwłaszcza dla pacjentów docelowych (DT), którzy do końca życia będą z urządzeniemfile-loesf2rt6rekhsjfhyskxufile-loesf2rt6rekhsjfhyskxu. Można przypuszczać, że takie programy (np. regularne warsztaty adaptacyjne co kilka lat) będą tam wdrażane, co może być inspirujące dla innych krajów. Holandia – znana z nowatorskiego podejścia do opieki zdrowotnej – postawiła na model zdecentralizowany: mniejsze szpitale są włączane w kontrolę pacjentów LVAD po odpowiednim przeszkoleniu personelu. Holendrzy kładą nacisk na edukację społeczną – np. organizują kampanie informacyjne o życiu z LVAD, aby otoczenie pacjenta (pracodawcy, służby ratunkowe, lokalna społeczność) rozumiało jego potrzeby. Francja – oprócz wysokiego poziomu opieki medycznej (kilka ośrodków paryskich ma wyniki 1-rocznego przeżycia >85%), wyróżnia się zaangażowaniem stowarzyszeń pacjentów. Francuskie stowarzyszenie pacjentów z sztucznym sercem i LVAD oferuje infolinię wsparcia psychologicznego, organizuje zjazdy i grupy dyskusyjne, gdzie wymieniane są dobre praktyki (np. jaki plecak najlepszy do noszenia baterii, jak radzić sobie z dyskomfortem latem). Takie partnerstwo organizacji pozarządowych z systemem opieki wzbogaca wsparcie formalne o cenny element peer support.
Podsumowując, wzorce z zagranicy pokazują, że kompleksowa opieka psychospołeczna nad pacjentem z LVAD jest możliwa i przynosi wymierne efekty: poprawę jakości życia, lepszą adherencję do zaleceń, mniejszą częstość powikłań oraz większą satysfakcję pacjentów i ich rodzin z procesu leczenia. Polska stoi u progu szerszego wdrożenia tej filozofii opieki – wymaga to połączenia sił środowiska medycznego (specjalistów wielu dziedzin), decydentów systemowych oraz samych pacjentów i opiekunów, by stworzyć środowisko sprzyjające nie tylko przeżyciu, ale i dobremu życiu z LVAD.
Podsumowanie
Opieka nad pacjentem z LVAD wykracza daleko poza aspekty techniczne i medyczne – jest to wyzwanie holistyczne obejmujące kondycję psychiczną chorego, jego relacje z bliskimi, jakość życia i zdolność adaptacji do nowej rzeczywistości. Niniejsza analiza przedstawiła kluczowe psychospołeczne problemy związane z terapią LVAD (depresja, lęk, stres opiekunów, zaburzenia adaptacyjne, obraz ciała, seksualność, radzenie sobie) oraz zarysowała wielopoziomowe strategie ich przezwyciężania. Najważniejsze zalecenia dla praktyki to: zapewnienie profesjonalnej oceny i wsparcia psychologicznego na każdym etapie (przed i po zabiegu), integracja psychologa w zespole LVAD, systematyczne monitorowanie samopoczucia pacjentów i opiekunów, wdrażanie interwencji indywidualnie dopasowanych (CBT, mindfulness, grupy wsparcia, rehabilitacja itp.) oraz organizacja opieki w sposób ciągły i skoordynowany. Doświadczenia zarówno polskie, jak i międzynarodowe dowodzą, że takie podejście się opłaca – cierpienie psychiczne pacjentów można skutecznie łagodzić, a w efekcie przekłada się to na twardsze wskaźniki kliniczne (mniej powikłań, dłuższe przeżycie)pubmed.ncbi.nlm.nih.gov. Niezbędne jest wsparcie systemowe dla tych działań, jednak już teraz wiele można osiągnąć dzięki świadomości i zaangażowaniu personelu w istniejących ramach. Jak wskazują eksperci, inwestycja w opiekę psychospołeczną jest inwestycją w jakość i efektywność leczenia. Zapewnienie pacjentom z LVAD – oraz ich rodzinom – kompleksowego, empatycznego wsparcia pozwala im nie tylko przeżyć, ale też żyć w pełni z nowym sercem mechanicznym. Jest to cel, do którego powinniśmy wspólnie dążyć, implementując najlepsze praktyki i stale doskonaląc nasze podejście.
Źródła:
- Milaniak I. i wsp. The experience of bodily image for patients with LVAD. Front. Psychiatry, 2025 – Wyniki badania dotyczącego obrazu ciała i jego związków z depresją/lękiem u pacjentów z LVAD.
- Bidwell J.T. i wsp. Patient and Caregiver Determinants of QOL and Caregiver Strain in LVAD Therapy. J. Am. Heart Assoc. 2018 – Badanie ukazujące wpływ charakterystyki opiekuna na wyniki pacjenta; wskazuje m.in. na wzrost obciążeń opiekunów w pierwszym miesiącu po LVAD.
- DeFilippis E.M. i wsp. Psychosocial Risk and Outcomes in CF-LVAD Patients. Circ Heart Fail. 2020 – Analiza ponad 15 tys. pacjentów z LVAD; ok. 20,5% miało ≥1 czynnik ryzyka psychospołecznego (ograniczone wsparcie, nałogi itp.), co wiązało się z częstszymi infekcjami, krwawieniami i rehospitalizacjamipubmed.ncbi.nlm.nih.govpubmed.ncbi.nlm.nih.gov.
- Morgenroth O. i wsp. Self‐compassion and psychological adjustment in LVAD patients. ESC Heart Failure, 2022 – Wykazano, że wyższa samo-współczucie koreluje z niższą depresją i lękiem u pacjentów LVAD; sugeruje potrzebę wzmacniania tego zasobu
- Kanellakis K. i wsp. Positive Psychology Intervention (PEACE) in LVAD patients. Psychology, 2022 – Badanie pilotażowe interwencji skupionej na wdzięczności i pozytywnych emocjach; odnotowano redukcję depresji i wzrost zadowolenia z życia.
- Levelink M. i wsp. Psychological burden and coping in destination therapy LVAD patients: a qualitative analysis. Artif Organs, 2022 – Wywiady z pacjentami długotrwale żyjącymi z LVAD; opisano główne obciążenia (fizyczne i psychospołeczne) oraz strategie radzenia sobie (problemowe – zarządzanie urządzeniem, emocjonalne – dystrakcja, „udawanie normalności”)file-loesf2rt6rekhsjfhyskxufile-loesf2rt6rekhsjfhyskxu.
- Scaglione A. i wsp. Short- and long-term effects of cardiac rehabilitation in LVAD patients. PLoS ONE, 2021 – Wykazało, że 4-tygodniowy program rehabilitacji poprawia jakość życia i wydolność fizyczną pacjentów z LVAD w stopniu podobnym jak u pacjentów po transplantacji; efekt utrzymuje się do 1 roku.
- Jaworska I. i wsp. Przygotowanie do implantacji mechanicznego wspomagania krążenia – aspekty psychiatryczne. Psychiatr. Polska, 2020 – Polski artykuł przeglądowy omawiający ryzyka psychiczne u pacjentów LVAD i zalecane postępowanie; podkreśla rolę przygotowania pacjenta i rodziny do terapiipsychiatriapolska.plpsychiatriapolska.pl.
- Wnioski z analizy własnej (2025) – Podsumowanie najnowszych danych naukowych oraz doświadczeń klinicznych dot. opieki psychospołecznej nad pacjentami z LVAD, m.in. z wykorzystaniem źródeł: Front. Psychiatry 2025, ESC Heart Failure 2022, Circ Heart Fail 2020, Artif Organs 2022, JAHF 2018, oraz wytycznych ISHLT 2023. Wszystkie powyższe dane jednoznacznie wskazują, że holistyczne wsparcie pacjenta i opiekuna stanowi integralny element skutecznej terapii LVAD.
